La pharmacogénomique: un outil de choix pour traiter le TDAH
Lorsqu’un enfant reçoit un diagnostic de trouble du déficit de l’attention avec ou sans hyperactivité (TDAH), il est possible de soulager ses symptômes. L’une des solutions consiste à lui prescrire un traitement pharmacologique en complément à d’autres stratégies. Le problème, c’est de trouver la bonne molécule au bon dosage pour que le traitement soit pleinement efficace. Plutôt que de s’en remettre uniquement à une approche traditionnelle essai-erreur, la pharmacogénomique fournit des renseignements qui peuvent guider le choix du médicament.
TDAH: une approche combinée de traitements
Pour obtenir de meilleurs résultats dans les soins du TDAH des enfants, une approche combinée est souvent préconisée. Elle repose souvent sur une combinaison de stratégies:
- la mise en place de stratégies comportementales;
- l’intégration de l’enfant dans un milieu scolaire approprié;
- l’établissement de routines et de saines habitudes (alimentation, sommeil, activité physique et temps d’écran);
- la prise de médicaments [1].
Les aléas de la prise de médicaments
Le choix de donner ou non un médicament à son enfant est une décision parentale très personnelle et difficile à prendre. De plus, parmi les nombreux médicaments qui peuvent aider un enfant vivant avec un TDAH, il n’est pas aisé de déterminer celui qui lui conviendra le mieux.
Le processus essai-erreur
Trouver la bonne molécule, le bon dosage ou la meilleure combinaison de traitements constitue parfois un travail de longue haleine. Si certains enfants ressentent les bénéfices de la médication au premier essai, d’autres doivent parfois s’armer de patience et traverser une longue série d’essais et d’erreurs.
De plus, pour traiter un type particulier de problème de santé, un médecin peut avoir recours à plusieurs médicaments, particulièrement en psychiatrie. D’autres facteurs comme les comorbidités (quand plus d’une maladie est présente à la fois, telle que le TDAH et l’anxiété) peuvent aussi influer sur le nombre de médicaments. La quantité d’options de médicaments peut donc augmenter rapidement, prolongeant le processus essai-erreur, comme en témoignent des études sur le traitement du trouble dépressif majeur:
- 2 patients sur 3 ne sont pas soulagés ou en voie de rémission après le 1ertraitement [2].
- 38% des patients répondent mal aux antidépresseurs inhibiteurs spécifiques du recaptage de la sérotonine (ISRS) [3].
- Les chances de succès diminuent après chaque nouvel essai de traitement [4].
Les effets secondaires
Par ailleurs, certains médicaments utilisés dans le traitement du TDAH peuvent entraîner des effets secondaires indésirables qu’aucun parent ne veut faire subir à son enfant:
- Perte d’appétit
- Irritabilité
- Maux de tête
- Troubles du sommeil
Pour limiter ces inconvénients, de plus en plus de médecins se tournent vers la pharmacogénomique, car elle peut les orienter dans le choix et le dosage d’un médicament.
En quoi consiste la pharmacogénomique?
Fusion des mots « pharmacologie » (étude des médicaments) et « génomique » (étude du génome), la pharmacogénomique étudie l’influence des gènes sur l’effet des médicaments. Elle a pour objectif de guider le choix de traitement et de réduire le processus essai-erreur [5].
Le métabolisme: normal, rapide ou lent
Michel Cameron, directeur adjoint en pharmacogénomique chez BiogeniQ, acquis par Biron en 2018, explique que «lorsqu’une pilule est ingérée, elle se dissout dans l’organisme pour produire son effet. Elle est aussi métabolisée, c’est-à-dire transformée par des enzymes (principalement situées dans le foie) pour faciliter son élimination».
Des dizaines d’enzymes différentes sont chargées du métabolisme, et chacune a ses préférences pour l’un ou l’autre des médicaments prescrits. Les enzymes mobilisées dépendent donc du médicament, et leur vitesse de réaction peut varier d’une personne à l’autre selon la génétique de chacun. On parle alors de métaboliseurs normaux, rapides ou lents, selon le cas. Voici les effets potentiels d’un médicament sur chaque type de métabolisme:
- Comparé à un métaboliseur normal (représentant la moyenne de la population avec laquelle les doses standards sont calculées), un métaboliseur rapide métabolise le médicament plus vite, ce qui peut faire en sorte qu’il n’est jamais exposé à des quantités suffisantes de médicaments pour produire l’effet thérapeutique escompté.
- Comparé à un métaboliseur normal, un métaboliseur lent prend plus de temps à métaboliser le médicament. Le médicament reste dans le corps plus longtemps et peut même s’accumuler à des niveaux très élevés, ce qui augmente les risques d’effets secondaires.
Le test génétique: pour prendre les devants
Grâce à un simple échantillon salivaire (qui ne demande aucune préparation particulière), le test pharmacogénomique vise à déterminer les vitesses de réaction des diverses enzymes responsables du métabolisme des médicaments. Les résultats permettent de savoir si des ajustements aux doses standards seraient justifiés ou même si certains médicaments devraient être évités pour limiter les risques de complications ou d’inefficacité [5].
Dans cette vidéo, Michel Cameron explique l’intérêt de la pharmacogénomique d’un point de vue thérapeutique.
https://www.youtube.com/watch?v=JqAPxXLBBiE
Un outil pour prescrire le bon traitement
Les enfants atteints de TDAH partagent souvent des symptômes similaires, mais chaque enfant est unique et doit recevoir un traitement adapté à son profil.
Certains médecins demandent un test pharmacogénomique avant de prescrire des médicaments afin d’obtenir des renseignements qui les aideront à personnaliser le traitement.
Ces tests fournissent de précieux renseignements sur la constitution génétique unique de l’enfant qui permettent de :
Évaluer les risques d’effets indésirables ou d’inefficacité
Les médicaments contre le TDAH se répartissent en deux catégories principales: les stimulants et les non-stimulants. Bien qu’ils puissent tous deux être utilisés pour traiter le TDAH, ils fonctionnent différemment, et les enfants ne réagissent pas tous de la même manière à chacun d’eux. La pharmacogénomique permet de donner un aperçu de la façon dont un médicament pourrait fonctionner selon la génétique d’un enfant.
Déterminer quelle dose de médicament prescrire
En déterminant le type de métabolisme du sujet (normal, lent ou rapide), il est possible de comprendre comment son corps décompose les médicaments. Il est alors possible de faire des ajustements de doses pour maximiser l’efficacité et causer le moins d’effets secondaires possibles.
Des marqueurs génétiques qui en disent long
Pour environ 70% des enfants ayant reçu un diagnostic de TDAH, les traitements de première ligne (psychostimulants à base de méthylphénidate ou d’amphétamine) réussissent rapidement à favoriser la concentration, un objectif recherché pour la majorité des enfants. Cependant, 30% sont réfractaires aux premiers traitements et requièrent plusieurs essais avant de trouver celui qui convient [6].
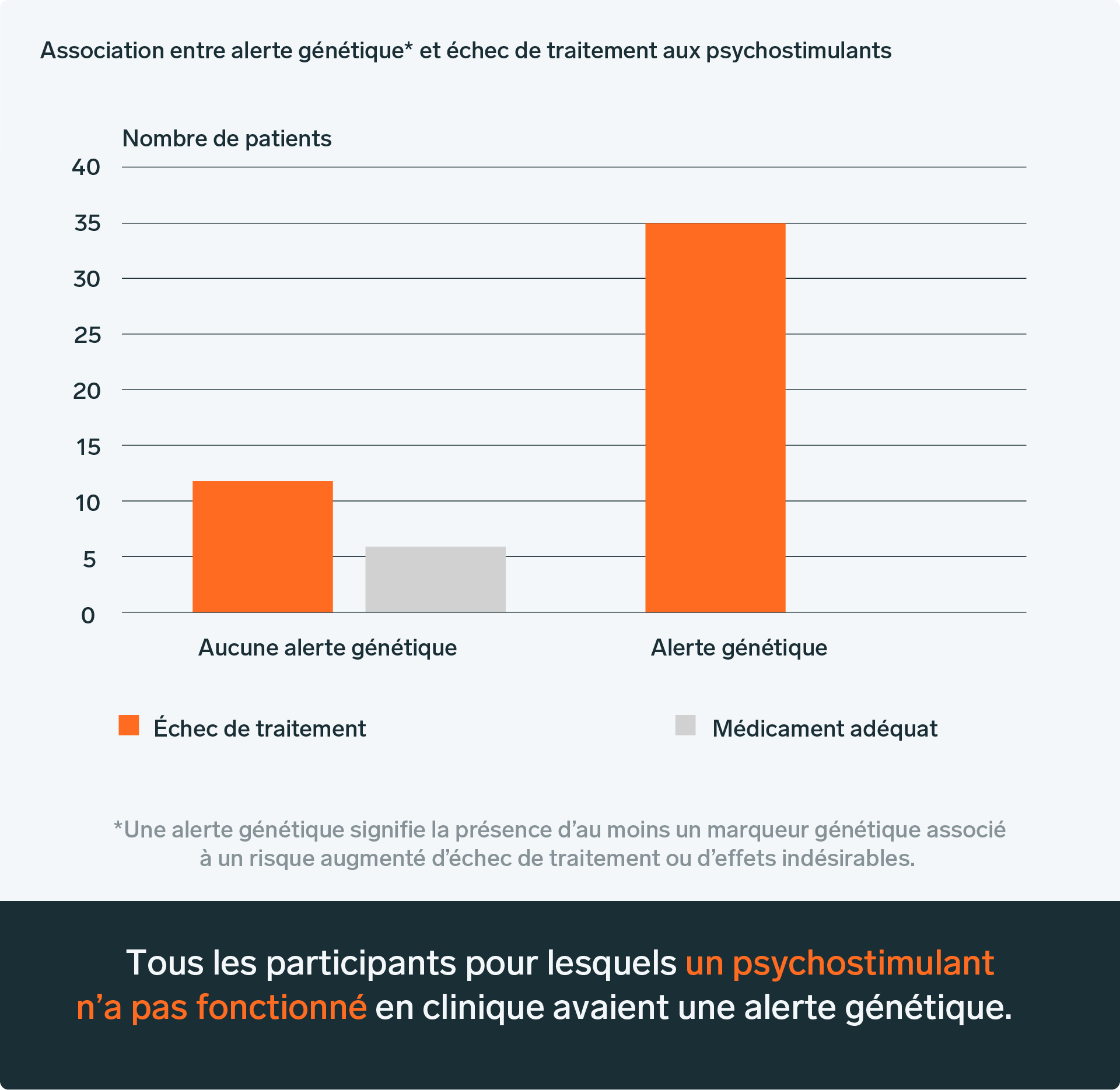
Afin de réduire le nombre d’essais de médicaments, le laboratoire BiogeniQ a réalisé en 2018 une étude rétrospective sur le traitement du TDAH. Elle a démontré une association entre les échecs de traitement et l’analyse pharmacogénomique. Ainsi, une alerte pharmacogénomique était toujours présente lorsqu’un traitement avait échoué par le passé, suggérant que le test pourrait être utile afin d’éviter des traitements inappropriés [7].
Une science prometteuse
Même si la pharmacogénomique est encore relativement nouvelle, elle n’en suscite pas moins un vif intérêt chez les praticiens et praticiennes en raison des importants bénéfices qu’elle procure.
Dr Chad Bousman, professeur de génétique médicale à l’Université de Calgary, dirige le projet PGx-SParK sur l’utilité de la pharmacogénomique pour les enfants ayant des problèmes de santé mentale. Il estime qu’une large portion du processus essai-erreur pourrait être évité grâce aux tests pharmacogénomiques. Ses études ont ainsi montré que la pharmacogénomique augmente de 41% les chances de rémission dans les cas de troubles dépressifs majeurs [8].
La pharmacogénomique offre aujourd’hui un outil supplémentaire à la médecine traditionnelle. Elle permet d’optimiser le processus essai-erreur et d’améliorer plus rapidement la condition des patients et patientes, notamment celle des enfants aux prises avec un TDAH.
BiogeniQ offre des services de pharmacogénomique qui peuvent aider votre médecin à évaluer les risques qu’un médicament pour traiter le TDAH cause des effets indésirables ou soit inefficace.
Sources :
[1] Société canadienne de pédiatrie. «Les médicaments contre le trouble de déficit de l’attention/hyperactivité», Soins de nos enfants, mai 2019, https://soinsdenosenfants.cps.ca/handouts/behavior-and-development/medications-for-attention-deficit-hyperactivity-disorder
[2] Trivedi, M. H. et coll. «Evaluation of outcomes with citalopram for depression using measurement-based care in STAR*D: implications for clinical practice», The American Journal of Psychiatry, vol. 163, no1, p. 28-40, 2006. https://ajp.psychiatryonline.org/doi/full/10.1176/appi.ajp.163.1.28
[3] Spear, B., M. Heath-Chiozzi, J. Huff. «Clinical application of pharmacogenetics», Trends in Molecular Medicine, vol. 7, no 5, p. 201-204, mai 2001.
http://pkmp.org.pl/assets/31/62/58/66acc37140612d12d81c8ea5b44d3bd33208e4ad.pdf
[4] Huynh, N.N., R. S. McIntyre. «What are the implications of the STAR*D Trial for primary care? A review and synthesis», Primary Care Companion to the Journal of Clinical Psychiatry, vol. 10, no 2, p. 91-96, 2008. https://www.psychiatrist.com/wp-content/uploads/2021/02/23874_are-implications-stard-trial-primary-care-review-synthesis.pdf
[5] Cameron, M. «La pharmacogénétique pour une médication plus ciblée», Biron Groupe Santé, 10 février 2022. https://www.biron.com/fr/centre-du-savoir/parole-de-specialiste/pharmacogenetique-medication-ciblee/
[6] Budur, K. et coll. «Non-Stimulant Treatment for Attention Deficit Hyperactivity Disorder», Psychiatry, vol. 2, no 7, p. 4-48, 2005. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3000197/
[7] Cameron, M. «Pharmacogénétique et TDAH – résultats positifs d’une étude rétrospective», Biron Groupe Santé, 6 novembre 2018. https://www.biron.com/fr/actualites/sante-a-a-z/pharmacogenetique-et-tdah-resultats-positifs-d-une-etude-retrospective/
[8] Brown, L.C., J.D. Stanton, K. Bharthi, A.A. Maruf, D.J. Müller, C.A. Bousman. «Pharmacogenomic Testing and Depressive Symptom Remission: A Systematic Review and Meta-Analysis of Prospective, Controlled Clinical Trials», Clinical Pharmacological & Therapeutics, vol. 112, no 6, p. 1303-1317, 2022. https://pubmed.ncbi.nlm.nih.gov/36111494/